Antioxidantien helfen, Krebs zu metastasieren
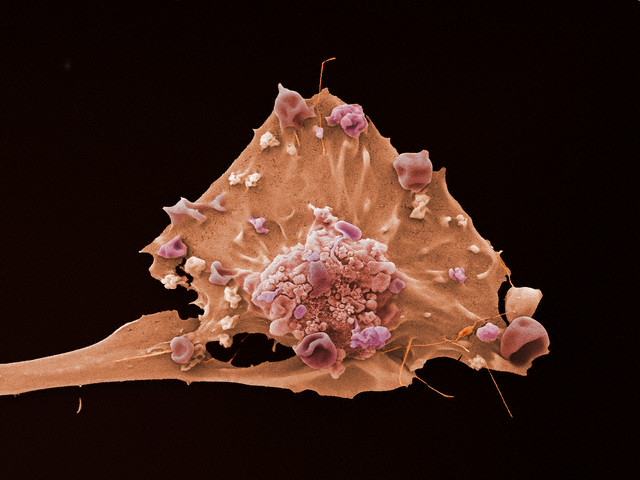
Brustkrebs-Zelle. (Photo Visuals Unlimited / Corbis) .
Arzneimittel zur Behandlung von Diabetes, das Niveau von oxidativem Stress senken und dadurch drängen Tumoren, Metastasen zu bilden.
Es ist bekannt, dass Sauerstoffradikale - sogenannte spezielle Moleküle, die Sauerstoff enthalten und die aufgrund des ungepaarten Elektron eine sehr hohe oxidative Wirkung haben - stark DNA schädigen können.
Wenn solche Reste viel wird, gibt es oxidativen Stress, und die Zelle kann sterben, oder einfach durch Mutationen, oder, sagen wir, die Krebs verursachen. Highly Sauerstoffoxidationsmittel werden als Nebenprodukt bestimmter wichtiger zellulärer Prozesse erhalten wird, so daß im Laufe der Evolution von Lebewesen Werkzeuge für ihre Entfernung sind.
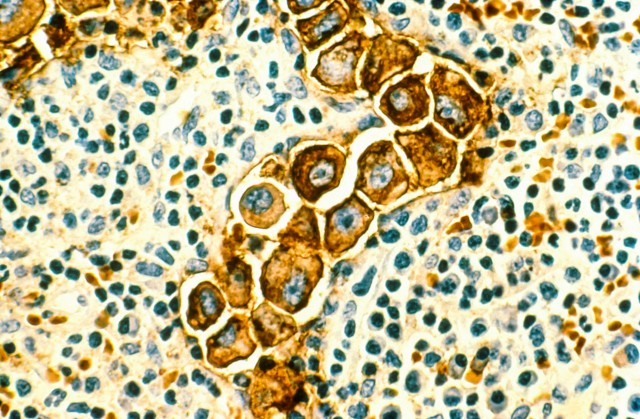
Lungenkrebszellen in den Lymphknoten. (Foto von NCI / Phanie / phanie / Phanie Sarl / Corbis) .
Allerdings kann die eingebaute in antioxidative Abwehrsystem nicht mit dem Problem fertig zu werden - und dann können sie durch den Verzehr von etwas Antioxidans Vorbereitung geholfen werden.
Aber auch Krebszellen, so lange, wie sie bereits erschienen sind, ist oxidativer Stress nicht benötigt. Wenn Krebs stark DNA zerstört wird, egal wie bösartig der Tumor sein kann, ist es nach wie vor zu sterben - in der Tat, die Masse von Anti-Krebs-Medikamente und hat genau das macht, dass eine Mutation in der DNA von Tumorzellen. Dann stellt sich heraus, dass Antioxidantien in die Hände von Krebs spielen, seine Gene so vor Schäden zu speichern. Es ist diese Logik in der Argumentation von James Watson war (denken Sie daran - einer der Autoren des legendären doppelsträngigen DNA-Modell), mit dem er öffentlich im Jahr 2013 sprach, sehr die Öffentlichkeit angesichts der populären Wissenschaft und populären Publikationen einfach peinlich. Doch Experten in den Worten von Watson war nichts Unerwartetes - wenn die breite Öffentlichkeit zu Onkologen für Kommentare gehetzt hat, zuckte sie mit den Schultern: sie sagen, über die Mehrdeutigkeit von Antioxidantien, haben wir lange bekannt gewesen. Ein Beispiel: im Jahr 1994 als Folge der groß angelegten Studie, die mehr als 29.000 Männer Raucher beteiligt sind, wurde festgestellt, dass der Krebs häufiger in diejenigen auftreten, die die Antioxidans Beta-Carotin-Pillen nahm. Im allgemeinen haben die Vorteile von Antioxidantien immer wieder in klinischen Versuchen zu testen versucht und in Tierversuchen, aber die Ergebnisse sind oft nicht die gleichen wie erwartet. Im gleichen 2013 der Zeitschrift der American Medical Association veröffentlicht einen Artikel, der erklärt , dass Vitamin E, Beta-Carotin und hohe Dosen von Vitamin A , um Ihre Chancen für einen vorzeitigen Tod erhöhen kann, unabhängig davon , ob Sie gesund oder krank ein -nibud chronische Erkrankung.
Ähnliche Arbeiten sind ein anständiges allmählich angesammelt, aber sie waren die Ergebnisse der medizinischen und statistischen Analyse, die nichts über die Mechanismen der Wirkung von Antioxidantien negativ gesagt. Doch nicht lange die molekularen "mechanistischen" Arbeit auf sich warten: 2014 Forscher von der Universität Göteborg berichtete über die Seiten von Science Translational Medicine , Antioxidantien, den Grad der Sauerstoffradikale reduziert, wodurch p53 ausgeschaltet, deren Mission - das Niveau der Mutation in einer Zelle zu überwachen. Wenn die Zelle in eine maligne Entartung droht, p53 löst die Apoptose - zelluläre Selbstzerstörungsprogramm. Im vergangenen Jahr machte die gleichen Autoren eine weitere Veröffentlichung Melanom betreffend - den Tumor und so bekannt ist für seine Neigung zur Metastasierung und Antioxidantien, wie sich herausstellte , mehr und das Auftreten von Melanom - Metastasen zu verbessern.
Der neue Artikel, die vor kurzem erschienen in Science Translational Medicine , sprechen wir über verschiedene Arten von Tumoren. Huntin Zheng (Hongting Zheng) und seine Kollegen aus der Dritten Military Medical University in Chongqing analysiert, um die Wirkung auf die Krebszellen von mehreren Anti-Diabetes-Medikamente, einschließlich Insulinanaloga und einigen berühmten Metformin. Diese Medikamente haben gemeinsam war, dass sie Enzyminhibitoren von Dipeptidylpeptidase Typ 4 (PID-4) und Alpha-Liponsäure enthalten. Und Dipeptidyl-Peptidase-Inhibitoren, und Alpha-Säure lipoevaaya Blutzucker zu reduzieren und dazu beitragen, die Unempfindlichkeit gegenüber Insulin zu überwinden (die zweite Art von Diabetes die Hauptsymptom).
Es wurde festgestellt, dass Antidiabetika Migration und Invasion des neuen Gewebes von metastatischen Zellen von Melanomen und Tumoren der Lunge, Darm-, Brust-, Eierstock- und Leber abstammen stimuliert. Wie die Autoren die Arbeit, die Zellteilung unterstreichen nicht beschleunigt wird, dh nur Medikamente, die Ausbreitung von Krebs beschleunigt, aber nicht seine Höhe (von denen jedoch nicht helfen). Die meisten der Versuche wurden in vitro in Zellkultur durchgeführt, aber nicht mit diesem Tumor in vivo, aber im Fall der Leber und Dickdarmkrebs von transplantierten Mäusen dann beobachtet, wie die Tumorzellen durch die Wirkung eines anti-diabetisches aktiven Streuung in gesunden Geweben.
Aber woher kommt die Antioxidantien? Erstens sich die Alpha-Liponsäure ist ein Antioxidans, zweitens zeigten weitere Experimente, daß Dipeptidyl-Peptidase-Inhibitoren auch das Niveau von oxidativem Stress in Krebszellen reduzieren. Und, was wichtig ist, wurden mit Metastasen verbunden ist, ist die antioxidative Wirkung von Arzneimitteln: wenn die Tumorzellen spezifisch die oxidativen Stress erhöht, sie nicht mehr aktiv aus dem Primärtumor zu migrieren, trotz der Anwesenheit von anti-diabetisches Substanzen mit antioxidativen Eigenschaften.
Die Forscher haben versucht, tiefer zu graben, und kam schließlich zu einem Transkriptionsfaktor namens NRF2. Transkriptionsfaktor genannt spezielle Proteine, die an bestimmte Sequenzen in der DNA binden, die Verbesserung oder Verringerung der Transkription - die Synthese von RNA-Kopien in dem gewünschten Gens. Es ist durch Transkriptionsfaktoren, nimmt der Anteil der regulatorischen Signale des Löwen, die genetische Aktivität zu kontrollieren. Es stellte sich heraus, dass alle Inhibitoren der Dipeptidyl-peptidase für den Versuch gemacht, Faktor NRF2 aktiviert, und dass seine Aktivierung Krebszellen induziert Umsiedlung - wenn NRF2 künstlich getrennt, metastasierende Tumoraktivität fiel, und seine Zellen erscheinen weniger Protein für die Reise erforderlich ist. Das heißt, das Ergebnis ist ein solches Schema: Inhibitoren der Dipeptidyl Peptidase in Arzneimitteln zur Behandlung von Diabetes enthalten ist, aufgrund seiner antioxidativen Wirkung auf den Transkriptionsfaktor NRF2 wirkt, und er, der wiederum "aufwacht" metastatic Genen. Ein weiteres Medikament Komponente, Alpha-Liponsäure, sagten die Forscher, funktioniert auf die gleiche Art und Weise.
Es ist interessant, dass etwa NRF2 war sich bewusst, dass seine Tätigkeit unter dem Einfluss von onkogenen Proteine erhöht wird, und dass er die Krebszellen benötigt oxidativen Stress zu löschen - das heißt, natürlich, aktiviert NRF2 nicht nur die "Migration" Gene und Antioxidans.
Es sollte betont werden, dass diese Medikamente, die metastatische Prozesse stimulieren Krebs verursachen nicht. Hier können wir die Arbeit der Forscher von der McGill University erinnern, veröffentlicht im Jahr 2012 in Cancer Prevention Research Artikel , in dem sie sagte , dass die Anti-Diabetes Metformin Tumoren verhindert - und es verhindert , dass sie da , dass oxidativer Stress reduziert. Das heißt, bis es keinen Krebs, Antioxidationsmittel tut gut zu ihm, und dann war es nicht, aber es ist nur die Krebszellen auftreten, ist der Effekt umgekehrt.
Wie auch immer, dass Diabetes und bösartigen Tumoren unter Berücksichtigung begleiten einander oft, gibt es ein Problem ist, wie man die richtige Therapie zu wählen. Hier ist natürlich, mehr Forschung ist notwendig, einschließlich klinischer, dass würde geschätzt werden, da die schädlichen Auswirkungen all dieser Medikamente auf die Dosis hängt - können hier und Probleme nicht vorhanden sind, wenn es sich herausstellt, dass die Antidiabetikum Eigenschaften der Medikamente bei niedrigeren Dosen erscheinen als die Fähigkeit eines Tumors zur Metastasierung zu schieben.
Via the-scientist.com


Kommentare
im Auge kommentierte halten , dass der Inhalt und der Ton Ihrer Nachrichten , die Gefühle von echten Menschen verletzen können, Respekt und Toleranz gegenüber seinen Gesprächspartnern, auch wenn Sie Ihr Verhalten in Bezug auf die Meinungsfreiheit und die Anonymität des Internets, ändert ihre Meinung nicht teilen, nicht nur virtuell, sondern realen Welt. Alle Kommentare werden aus dem Index, Spam - Kontrolle versteckt.