| Teil Heim
Produktion, Amateur Funkamateur Modellflugzeuge, Raketen- Nützlich, unterhaltsam |
Stealth - Master
Elektronik Physik der Technik Erfindung |
Raum Geheimnis
Erde Mysteries Secrets of the Ocean List Kartenausschnitt |
|
| Verwendung des Materials ist für die Referenz (für Websites - Hyperlinks) zulässig | |||
Navigation: => |
Startseite / Produkte Patente / In der Sektion des Kataloges / zurück / |
|
Erfindung
Russische Föderation Patent RU2284184
![]()
VERFAHREN ZUR BEHANDLUNG VON KREBS Speiseröhre und des Magens
Name des Erfinders: EDZHENI Dzhefferhazen A. (US); Steven E. Benner (US); DAGEN Terry S. (US)
Der Name des Patentinhabers: Bristol-Myers Squibb Company (US)
Korrespondenzanschrift: 119034, Moskau, Prechistenskiy Spur, 14, Gebäude 1, Etage 4, "Goulingz International Inc." Yu.V.Dementevoy.
Startdatum des Patents: 2002.03.04
Die Erfindung stellt ein Verfahren zur Krebs des Ösophagus, Krebs der Speiseröhre oder des Magens Verbindung oder Magenkrebs bei Menschen zu behandeln. Das Verfahren umfaßt eine Kombination aus Tegafur und Uracil mit Tegafur Dosis von 100-500 mg / m 2 / Tag in einem Molverhältnis von Tegafur und Uracil 1 oral verabreicht: 4; Die orale Verabreichung von 0,1-500 mg / kg / Tag von Folinsäure oder ein pharmazeutisch annehmbares Salz davon; intravenöser Verabreichung von Paclitaxel und Carboplatin in einer Dosis von 10-300 mg / m 2 und 100-500 mg / m 2 bzw. und Paclitaxel und Carboplatin sind an 1 Tag 28-tägigen Zyklus und Tegafur, Uracil und Folinsäure oder eines pharmazeutisch verträglichen verabreicht Salz - in den 2-22-ten Tage. Und die 23-28-ten Tag des Zyklus machen eine Pause. Bei diesem Behandlungsschema wird mindestens einmal wiederholt. Die Erfindung stellt eine wirksame Behandlung von Krebs und eine gute Verträglichkeit, indem die Aktivität von Paclitaxel und Carboplatin in Kombination mit den obigen Arzneimitteln zu erhöhen und eine sanftere und das Verabreichen einer Chemotherapie im Vergleich zu bekannten Verabreichungswege.
BESCHREIBUNG DER ERFINDUNG
Die vorliegende Erfindung umfasst die Verabreichung an einen Warm Kombination aus Tegafur, Uracil, Folinsäure, Paclitaxel und Carboplatin bei der Behandlung von Tumoren.
5-Fluorouracil (5-FU) ist ein bekanntes Antitumormittel. Die Kombination von 5-Fluorouracil und Folinsäure ist für die Behandlung von Darmkrebs bekannt. Tegafur (1- (2-Tetrahydrofuryl) -5-fluoruracil) ein Prodrug von 5-Fluoruracil. In vivo wird 5-Fluorouracil schnell durch das Enzym Dihydropyridin-Dehydrogenase (DPD) inaktiviert. Uracil hemmt DPD Metabolismus von 5-FU, von Tegafur gebildet. So kann die gleichzeitige Verabreichung von Tegafur, Uracil und führt zu mehr verlängerte Wirkung der aktiven 5-FU im Vergleich allein Tegafur. Es ist bekannt, daß 5-Fluorouracil kann nicht oral verabreicht werden.
U.S. Patent 4328229 beschreibt eine Anti-Krebs-Zusammensetzung, 1- (2-Tetrahydrofuryl) -5-fluoruracil ( "Tegafur") und Uracil enthält. Die Zusammensetzung wird für die Abgabe von 5-Fluoruracil an einen Tumor empfindlich auf 5-Fluorouracil, in warmblütigen Tieren eingesetzt. Es zeigt an, dass die Zusammensetzung kann in einer Vielzahl von Dosierungsformen, einschließlich einer oralen Dosierungsform verabreicht werden.
U.S. Patent 5534513 offenbart Tegafur und Uracil in einem Molverhältnis von 1 Antitumor-Zusammensetzung, enthaltend: 4 beträgt. Es wird behauptet, dass die Anti-Tumor-Zusammensetzung aktiver, wenn davon Folinsäure oder ein pharmazeutisch annehmbares Salz verabreicht werden können. Dieses Patent gibt an, daß die beschriebene Kombination in verschiedenen Dosierungsformen verabreicht werden, einschließlich oral.
Paclitaxel (Taxol), Diterpene Taxan-Serie, ist eine natürliche Substanz isoliert aus der Rinde der pazifischen Eibe, Taxus brevifolia. Studien haben gezeigt, dass es eine ausgezeichnete Antitumor-Aktivität gegen Tumore in vivo in einer Reihe von Tiermodellen besitzt, einschließlich beispielsweise Brust- und Eierstocktumoren. Paclitaxel ist ein antimitotische Mittel, das hauptsächlich an Mikrotubuli bindet. Die Stabilisierung von Mikrotubuli durch Paclitaxel hemmt Reorganisation des Mikrotubuli-Netzwerk. Paclitaxel wird typischerweise durch intravenöse Injektion oder Infusion verabreicht.
Carboplatin (PARAPLATIN®) ist ein bekanntes Antitumormittel, das eine Vernetzung der DNA induziert mit Proteinen und Nicht-Protein assoziiert ist. Dieser Effekt ist nicht spezifischen Zellzyklus. Carboplatin wird typischerweise durch intravenöse Infusion oder Injektion verabreicht.
Die Anmelder haben gefunden, daß 5-Fluorouracil, die Aktivität von Paclitaxel und Carboplatin verbessern. Jedoch aufgrund der Tatsache, dass 5-Fluorouracil nicht oral verabreicht werden kann, ist diese Kombination notwendig weniger schonend einzuführen, beispielsweise durch intravenöse Injektion, wie es in der Regel ein geschultes medizinisches Personal erfordert.
Es wäre höchst wünschenswert, ein Verfahren zur Behandlung von Tumoren bereitzustellen, insbesondere Tumoren des Ösophagus, der Speiseröhre und des Magens mit den Verbindungen der Magen, die eine intravenöse Verabreichung von Paclitaxel und Carboplatin, und die orale Verabreichung von 5-Fluorouracil zu einem Warmblüter für die wirksame Behandlung solcher Tumoren verbunden wäre.
ZUSAMMENFASSUNG DER ERFINDUNG
Diese Erfindung betrifft ein Verfahren zur Behandlung von Speiseröhrenkrebs oder Speiseröhrenkrebs Kopplungsbereich, Magen- oder Magenkrebs bei Menschen. Das Verfahren umfaßt eine Kombination aus Tegafur und Uracil mit Tegafur Dosis von 100-500 mg / m 2 / Tag in einem Molverhältnis von Tegafur und Uracil 1 oral verabreicht: 4; oral 0,1-500 mg / kg / Tag von Folinsäure oder ein pharmazeutisch annehmbares Salz davon; Paclitaxel und Carboplatin intravenös in einer Dosis von 10-300 mg / m 2 und 100-500 mg / m 2 bzw. und Paclitaxel und Carboplatin sind an 1 Tag 28-tägigen Zyklus und Tegafur, Uracil und Folinsäure oder eines pharmazeutisch annehmbaren Salzes verabreicht davon - in den 2-22-ten Tage, und 23-28 Tage des ersten Zyklus ist Pause.
Falls erforderlich, wird das Behandlungsschema mindestens einmal wiederholt.
DETAILLIERTE BESCHREIBUNG DER ERFINDUNG
Die Kombination aus Tegafur und Uracil in Mengen, die ausreichend Tegafur zu 5-Fluoruracil umzuwandeln (vorzugsweise ein molares Verhältnis von etwa 1: 4). Es kann oral verabreicht werden. Es wurde festgestellt, daß die orale Verabreichung dieser Kombination ausreichende Menge an 5-Fluoruracil hergestellt und zusammen mit Paclitaxel und Carboplatin ist eine aktive und wirksame Behandlung von Tumoren, vor allem diejenigen, vorgesehen. In die Speiseröhre und des Magens mit der Verbindung in den Magen mit Tumoren des Ösophagus verbunden.
In einer oralen Darreichungsform der vorliegenden Erfindung, Tegafur, Uracil und Folinsäure, vorzugsweise in Form von Calcium "Calciumfolinat" sind in der gleichen Salze orale Darreichungsform. Anderenfalls und vorzugsweise Tegafur und Uracil in einer ersten oralen Dosierungsform, und Folinsäure, vorzugsweise in Form von Calciumfolinat, wird in der zweiten oralen Dosierungsform enthalten. Die Dosis jedes Wirkstoffs pro Tag verabreicht wird, etwa 0,1-100 mg / kg / Tag, vorzugsweise etwa 1-30 mg / kg / Tag für Tegafur. Uracil in einer Dosis von etwa 1-50 mg / kg / Tag verabreicht. UFT Dosis, nämlich die Kombination von 1: 4 Tegafur und Uracil ist etwa 100-500 mg / m / Tag bezogen auf Tegafur, vorzugsweise von etwa 200-300 mg / m 2 / Tag , bezogen auf Tegafur. Folinsäure oder ein pharmazeutisch annehmbares Salz davon kann in einer Menge von etwa 0,1-500 mg / kg / Tag verabreicht werden, wird jedoch vorzugsweise als Calciumfolinat in einer festen Dosis von etwa 90 mg / Tag verabreicht wird. Die orale Dosierungsform (en) kann in einer Einzeldosis oder in aufgeteilten Dosen typischerweise bis zu 3 mal pro Tag verabreicht werden.
Paclitaxel und Carboplatin wird vorzugsweise oral verabreicht man nicht, ist es besser ist, sie durch intravenöse Infusion einzugeben. In Abhängigkeit von der Körperoberfläche von Paclitaxel Infusionsdosis kann von etwa 10 bis 300 mg reichen / m 2, vorzugsweise von etwa 30 bis 200 mg / m 2, und besonders bevorzugt etwa 100, 135 oder 175 mg / m 2. Vor der Infusion von Paclitaxel sollte in der Technik bekannt Vorbehandlung durchgeführt werden. Paclitaxel-Dosis wird vorzugsweise intravenös durch Infusion über einen Zeitraum von mindestens etwa 3 Stunden, vorzugsweise etwa 3 oder 24 Stunden verabreicht. Carboplatin Dosis wird vorzugsweise intravenös durch Infusion, vorzugsweise für mindestens etwa 15 Minuten verabreicht. Die Infusion von Carboplatin Dosis kann etwa 100-500 mg / m 2, bevorzugt etwa 300-360 mg / m 2 betragen. Und Infusion können die Carboplatin-Dosis Calvert Formel als AUC, von etwa 4-6 mg / ml * min berechnen.
Der Fachmann auf dem Gebiet kann bestimmen die Dosis über UFT, Folinsäure oder ein pharmazeutisch verträgliches Salz davon, Paclitaxel, beispielsweise auf Basis der Körperoberfläche und / oder unter Berücksichtigung der Toxizität von Carboplatin und Calvert Formel wie unten beschrieben. Gemäß der vorliegenden Erfindung wird die Kombination aus Tegafur und Uracil (z.B. UFT) mit Paclitaxel und Carboplatin eine ausreichende Menge an 5-Fluoruracil in Kombination stellt eine wirksame Behandlung von Tumoren zu erzielen, insbesondere Tumoren des Ösophagus, der Speiseröhre und des Magens -Verbindungen Verfahren Magen schonen.
, Typischerweise basierend auf einem 28-Tage-Zyklus gemäß einer bevorzugten Ausführungsform stellt die Erfindung ein Verfahren zur Behandlung von Krebs, insbesondere Krebs-Tumoren in einem warmblütigen Säuger, die die Wirkstoffe nach dem Schema umfasst. Beispielsweise Paclitaxel mit einer Dosis von etwa 100, 135 oder 175 mg / m 2, vorzugsweise etwa 175 mg / m 2, und Carboplatin in einer Dosis von etwa 300-360 mg / m 2, oder in einer Dosis auf den gewünschten Wert der Fläche unter der Konzentrationskurve (AUC) entspricht , gleich 4,6 mg / ml-min, vorzugsweise etwa 6 mg / ml-min, der Calvert Formel bestimmt, die jeweils 1 eines 28-tägigen Zyklus am Tag verabreicht werden, und UFT in einer Dosis von etwa 200, 250 oder 300 mg / m 2 / Tag auf Basis von Tegafur und Calciumfolinat mit einer Dosis von etwa 90 mg / Tag kann täglich für 2 th verabreicht werden - 22 th Tag, während die Wirkstoffe am Tag verabreicht werden , nicht 23-28. Falls erforderlich, eine 28-Tage-Zyklus wird wiederholt. Die Dosis von Carboplatin wird berechnet für jeden Verlauf der Therapie Calvert Formel vor:
Carboplatin in mg (Gesamtdosis) = (gewünschte AUC) × (GFR + 25)
AUC erforderlich ist etwa 4-6 mg / ml * min. Die Rate der glomerulären Filtrations (GFR in ml / min) wird durch Messung der Kreatinin-Clearance angenähert (Cr. Cl.) Des Patienten, die sich auf das Alter des Patienten (Jahre), Gewicht (kg) und der Gehalt an Kreatinin im Serum (mg / dl) ist abhängig von der Formel Krokrofta-Gault:
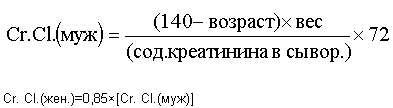
Die Dosierungsformen können hergestellt werden, beispielsweise unter Verwendung von herkömmlichen festen oder flüssigen Vehikeln oder Verdünnungsmitteln und pharmazeutischen Zusatzstoffen und in Abhängigkeit von der Art der Verabreichung (beispielsweise Exzipienten, Bindemittel, Konservierungsmittel, Stabilisatoren, Geschmacksstoffe, etc.) durch Verfahren in der Technik bekannt ist Apotheke.
Dosierungsformen zur oralen Verabreichung umfassen Tabletten, Pulver, Granulate, usw. Exzipienten und Additive, die verwendet werden können, umfassen, sind aber nicht beschränkt auf, Lactose, Sucrose, Natriumchlorid, Glucose, Harnstoff, Stärke, Calcium, Kaolin, kristalline Cellulose, Salicylsäure, Methylcellulose, Glycerin, Natriumalginat, Gummi usw. Man kann herkömmliche Bindemittel verwendet werden, wie beispielsweise Glucoselösungen, Stärkelösungen, Gelatinelösungen, usw. Sprengmittel schließen ein, sind jedoch nicht beschränkt auf trockene Stärke, Natriumalginat, Agar-Pulver, Calciumcarbonat usw. beschränkt Sorbentien können umfassen, sind aber nicht beschränkt auf, Stärke, Lactose, Kaolin, Bentonit, usw. Schmiermittel schließen ein, sind aber nicht beschränkt auf, gereinigter Talk, Stearinsäuresalze, Borsäurepulver, Polyethylenglykol usw. beschränkt
Dosierungsformen für die parenterale Verabreichung, wie subkutane, intravenöse, intramuskuläre oder durch Injektion in den Brustbeins oder durch Infusion, umfassen injizierbare Lösungen oder Suspensionen, welche zum Beispiel pharmazeutisch verträgliche Verdünnungsmittel oder Lösungsmittel, wie Mannit, 1,3-Butandiol, Wasser, Ringer-Lösung, isotonische Kochsalzlösung oder andere geeignete Dispersions- oder Benetzungs- und Suspensionsmittel, einschließlich synthetischer Mono- oder Diglyceride, und Fettsäuren, einschließlich Ölsäure.
Die folgenden Beispiele veranschaulichen die Erfindung, sind jedoch nicht zu deren Einschränkung gedacht.
Beispiel 1
Diese Studie bewertet die in-vivo-Dosis-limitierende Toxizität von UFT (Tegafur und Uracil in einem Mol-Verhältnis von 1: 4) und Calciumfolinat als 3-mal täglich für 21 Tage zu nehmen und in Kombination mit Taxol (Einzeldosis, infundiert über 3 Stunden im ersten Tag des Zyklus) und PARAPLATIN® (Einzeldosis, über 1 Stunde in einem Zyklus 1 Tag infundiert) bei Patienten mit Krebs der Speiseröhre, der Magen oder die Speiseröhre in den Magen und die Verbindung, die empfohlene Dosis zu bestimmen, verwendet werden, in der Phase II der Studie.
Eine Standard Phase I mit eskalierenden Dosen von UFT mit einer festen Dosis von Calciumfolinat (Leucovorin), gleich 90 mg / Tag, feste Dosis Taxol, gleich 175 mg / m 2 verabreicht als Infusion über 3 Stunden am Tag 1 durchgeführt wurde, und dosis PARAPLATIN®, die entsprechende Fläche unter dem erforderlichen Wert (AUC) -Kurve von etwa 6 mg / ml * min aus der Formel durch Infusion über 1 Stunde verabreicht Calvert berechnet. Die Anfangsdosis von UFT betrug 200 mg / m 2 / Tag auf Basis von Tegafur mit Leucovorin 90 mg / Tag verabreicht wurde, und beide Mittel Dosis wurde in 3 Dosen aufgeteilt und für 21 Tage verabreicht , beginnend an Tag 2, dann gefolgt von einem 6-tägigen Pause.
UFT Dosis von 3 bis 6 Gruppen von Patienten erhöht. Dosis Leucovorin-Regime und blieb unverändert. Eine Erhöhung der Dosis von UFT wurde durchgeführt, bis, bis ![]() 1 der ersten 3 Patienten oder
1 der ersten 3 Patienten oder ![]() 2 von 6 Patienten nicht beginnen Toxizität (maximal zulässige Dosis limitierende Toxizität) zu fühlen. Unmittelbar nach der reduzierten Dosis, die maximal verträgliche Dosis (MTD), empfohlen für Phase-II-Erfahrung.
2 von 6 Patienten nicht beginnen Toxizität (maximal zulässige Dosis limitierende Toxizität) zu fühlen. Unmittelbar nach der reduzierten Dosis, die maximal verträgliche Dosis (MTD), empfohlen für Phase-II-Erfahrung.
Gruppen von mindestens 3 Patienten wurden nach einer Dosis von UFT verabreicht: 200 (DL200), 250 (DL250) oder 300 (DL300) mg / m 2 / Tag , bezogen auf Tegafur.
Kriterien für die Studie umfassen, sind aber auf, histologisch oder zytologisch bestätigt metastasiertem oder inoperablem, lokal Plattenepithelkarzinom oder Adenokarzinom des Ösophagus, oder Gurgel-Verbindung mit dem Magen oder Adenokarzinom des Magens, Strahlentherapie zur gleichen Zeit für Tumoren metoznyh Status ECOG 0- Chemotherapie nicht beschränkt nicht nicht eingegangen 2 wurde in Hirnmetastasen und damit verbundene Störungen hämatologischen, Leber- und Nierenfunktionen beobachtet.
Die Behandlung wurde für 4 Wochen durchgeführt, solange es nicht Krankheitsprogression oder inakzeptabler Toxizität beobachtet wurden. TAXOL ® wurde 3 Stunden lang durch PARAPLATIN® gefolgt infundiert, intravenös in einer Dosis auf die Fläche unter der Kurve (AUC) entspricht etwa 6 mg / ml * min als 1 jedes Zyklus von der Calvert Formel Tag bestimmt. oral UFT und Leucovorin in der 2-22-ten Tag jedes Zyklus, gefolgt von einem 6-tägigen Pause dann verabreicht. Die Anfangsdosis von UFT betrug 200 mg / m 2 / Tag , bezogen auf Tegafur, wurde täglich in drei Portionen verabreicht. Leucovorin Dosis wurde bei 90 mg / Tag festgelegt, wobei die drei Teile gleichzeitig mit UFT 8-Stunden-Intervallen. Behandlungszyklen wurden alle 28 Tage wiederholt.
PARAPLATIN® Dosis wurde vor für jeden Patienten zu jeder Therapieverlauf berechnet, um die folgenden Verfahren. Calvert Formel verwendet:
PARAPLATIN® in mg = (erforderlich AUC) × (GFR + 25)
AUC benötigte Menge beträgt ca. 6 mg / ml * min. Geschwindigkeitswert glomerumernogo Filtration (GFR in ml / min) wurden durch die Messung der Kreatinin-Clearance angenähert (Cr. Cl.) Des Patienten, die auf der Grundlage von Alter (Jahre) bestimmt wird, das Gewicht in Kilogramm, und Serum-Kreatinin in mg / dL bei einem Patienten durch die Formel Krokrofta -Gaulta:
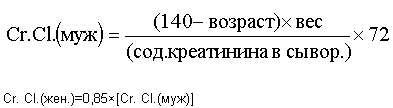
Nachdem alle Patienten erfolgreich einen Behandlungszyklus durchlief, wurde die Dosis von UFT erhöht. Die Studie zu jeder progressive Ebene fortgesetzt, es war noch nicht erreicht die maximal verträgliche Dosis (MTD). MTD wurde als die Dosis definiert, bei dem 1/3 oder mehr als 2/6 der Patienten fühlten dosislimitierende Toxizität (DLT) während des ersten Behandlungszyklus.
DLT wurde wie folgt bestimmt:
Hämatologische Toxizität:
- Neutropenie Grad 3/4 kompliziert durch Fieber begleitet, oder
- Thrombozytopenie Grad 3/4 durch Blutung oder Thrombozytentransfusionsbedürftigkeit kompliziert, oder
- Thrombozytopenie 4 Grad.
Nicht-hämatologische Toxizität:
- Übelkeit mehr als 3 Grad, Erbrechen, Durchfall trotz medizinischer Intervention, oder
- eine andere Art von hämatologischen Toxizität mehr als Grad 3 oder
- Unfähigkeit zu erhalten
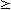 75% der geplanten Dosis UFT / Leucovorin oder
75% der geplanten Dosis UFT / Leucovorin oder - Verzögerung zu Beginn des nächsten Zyklus von mehr als 2 Wochen.
Die Patienten wurden in das Protokoll aufgenommen, wenn sie die folgenden Kriterien erfüllt werden:
- histologisch oder zytologisch metastasiertem oder inoperablem, lokal Plattenepithelkarzinom oder Adenokarzinom des Ösophagus, oder Gurgel-Verbindung mit dem Magen oder Adenokarzinom des Magens bestätigt;
- meßbare (> 1,5 cm in beiden Dimensionen) oder eine merkliche Erkrankung (
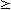 1,5 cm in mindestens einer Dimension);
1,5 cm in mindestens einer Dimension); - durch geeignete hämatologischen, Leber- und Nierenfunktion gekennzeichnet ist;
- Alter> 18 Jahre;
- Sie sind nicht auf eine der Chemotherapie oder Immuntherapie, einschließlich Hilfs und nevspomogatelnuyu Teil der Behandlung unterzogen wird;
- Der Status ECOG 0-2 (auf einer Skala Zubroda), Lebenserwartung> 3 Monate;
- schriftliche Zustimmung.
Die Patienten wurden ausgeschlossen, wenn sie jede Bedingung einen Darmverschluss oder beobachtet hatte, die die Absorption von UFT und / oder Leucovorin verhindert, oder waren vorher Sitzungen der Strahlentherapie, solange sie nicht mit palliativen oder adjuvanten Behandlung von metastasiertem oder lokalisierten bösartigen Adenokarzinom oder Plattenepithelkarzinom Ösophaguskarzinom Feld zugeordnet wurden Verbindung der Speiseröhre mit dem Magen oder dem Magen.
16 Patienten nahmen an Phase-I erfahren. Dosislimitierende Toxizität wurde während des Zyklus 1 bei zwei Patienten beobachtet. Bei DL200, ein Patient Grad 3 Übelkeit und Erbrechen erlebt, zu einem Verlust von 32% der Dosen von UFT führt, wenn DL300, ein Patient Grad 3 Myalgie. DL300 als verträgliche Dosis gesehen, und es erhielt 9 Patienten. Während des Zyklus 2 die negativen Auswirkungen mit einem DLT verbunden sind, wurde bei einem Patienten beobachtet, die mit Fieber neytropeniynoy auf mehr als 14 Tage Verzögerung der Thrombozyten Erholung entspricht, bei einem Patienten mit Grad 3 Müdigkeit, und ein Patient mit Grad 3 Erbrechen. In allen Zyklen, andere negative Symptome ![]() Grade 3 sind Fieber, Neutropenie, Neuropathie, tiefe Venenthrombose, Schüttelfrost, Erbrechen, Verstopfung und Müdigkeit. Klinische Antworten enthalten: partielles Ansprechen bei 6 Patienten beobachtet, bei denen eine Abnahme des Tumors war in der Regel mindestens 50%; stabile Erkrankung bei 4 Patienten beobachtet wurde, wo keine Änderung der Krankheit gibt (von weniger als 50% oder eine Erhöhung der Tumorgröße von weniger als 25%, dh eine Verringerung der Tumorgröße) ist. Fortschreiten der Erkrankung wurde bei 5 Patienten beobachtet. In dieser Gruppe waren neue, bisher nicht identifizierte Läsionen oder malignen pleuralen Efflux aufgetreten oder Aszites und / oder zumindest um 25% in der Menge von einem oder mehreren sichtbaren Läsionen erhöht. Das Behandlungsschema oben beschrieben wurde im Allgemeinen gut vertragen und anti-Tumor-Aktivität in allen Dosierungen demonstriert. Ein Patient konnte die Reaktion zu bestimmen.
Grade 3 sind Fieber, Neutropenie, Neuropathie, tiefe Venenthrombose, Schüttelfrost, Erbrechen, Verstopfung und Müdigkeit. Klinische Antworten enthalten: partielles Ansprechen bei 6 Patienten beobachtet, bei denen eine Abnahme des Tumors war in der Regel mindestens 50%; stabile Erkrankung bei 4 Patienten beobachtet wurde, wo keine Änderung der Krankheit gibt (von weniger als 50% oder eine Erhöhung der Tumorgröße von weniger als 25%, dh eine Verringerung der Tumorgröße) ist. Fortschreiten der Erkrankung wurde bei 5 Patienten beobachtet. In dieser Gruppe waren neue, bisher nicht identifizierte Läsionen oder malignen pleuralen Efflux aufgetreten oder Aszites und / oder zumindest um 25% in der Menge von einem oder mehreren sichtbaren Läsionen erhöht. Das Behandlungsschema oben beschrieben wurde im Allgemeinen gut vertragen und anti-Tumor-Aktivität in allen Dosierungen demonstriert. Ein Patient konnte die Reaktion zu bestimmen.
FORDERUNGEN
Verfahren für Speiseröhrenkrebs oder Speiseröhrenkrebs Feld Verbindung Magen oder Magenkrebs in einem Menschen , umfassend die Behandlung oral eine Kombination von Uracil und Tegafur, Tegafur in einer Dosis von 100 bis 500 mg / m 2 / Tag in einem Mol - Verhältnis von Tegafur und Uracil 1 Verabreichung: 4; oral 0,1-500 mg / kg / Tag von Folinsäure oder ein pharmazeutisch annehmbares Salz davon; Paclitaxel und Carboplatin intravenös in einer Dosis von 10-300 mg / m 2 und 100-500 mg / m 2 bzw. und Paclitaxel und Carboplatin sind an 1 Tag 28-tägigen Zyklus und Tegafur, Uracil und Folinsäure oder eines pharmazeutisch annehmbaren Salzes verabreicht davon - in den 2-22-ten Tage, und 23-28 Tage des ersten Zyklus ist Pause.
Verfahren nach Anspruch 1, wobei der Behandlungsplan mindestens einmal wiederholt wird.
Druckversion
Erscheinungsdatum 27.11.2006gg




Kommentare
im Auge kommentierte halten , dass der Inhalt und der Ton Ihrer Nachrichten , die Gefühle von echten Menschen verletzen können, Respekt und Toleranz gegenüber seinen Gesprächspartnern, auch wenn Sie Ihr Verhalten in Bezug auf die Meinungsfreiheit und die Anonymität des Internets, ändert ihre Meinung nicht teilen, nicht nur virtuell, sondern realen Welt. Alle Kommentare werden aus dem Index, Spam - Kontrolle versteckt.